Хотя некоторые полагают, что температура плавления такого сплава будет находится где-то между темпе-
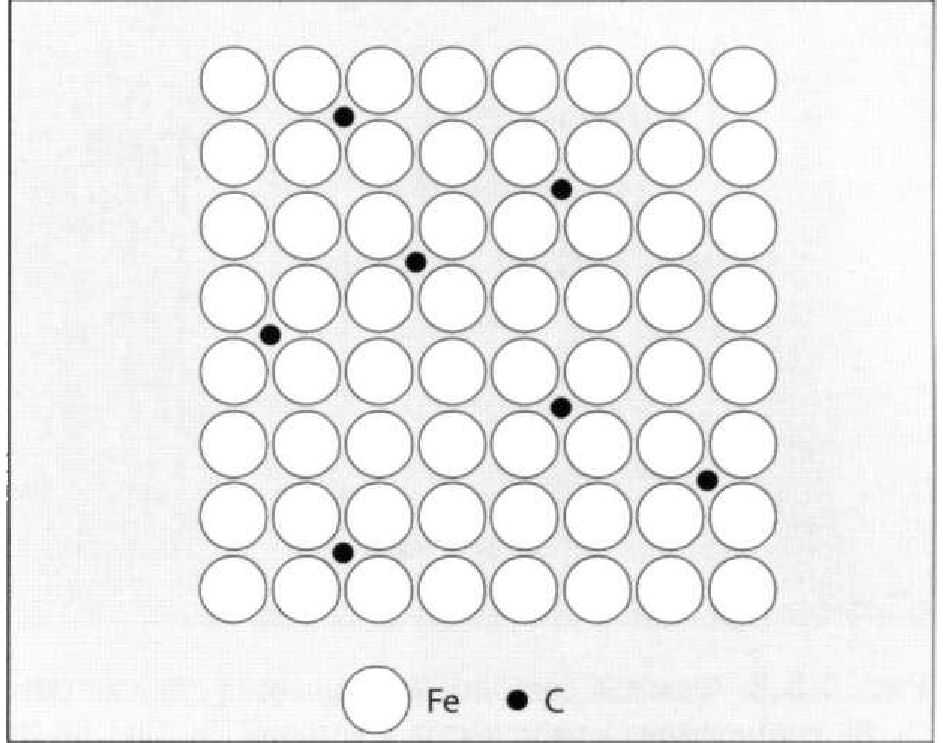
Рис. 1.5.7. Схематичное представление структуры твердого раствора внедрения
амальгам: в сплаве для амальгамы могут содержаться фазы Ag — Sn (Ag
3
Sn), а также, фазы Си — Sn (Cu
6
Sn
g
).
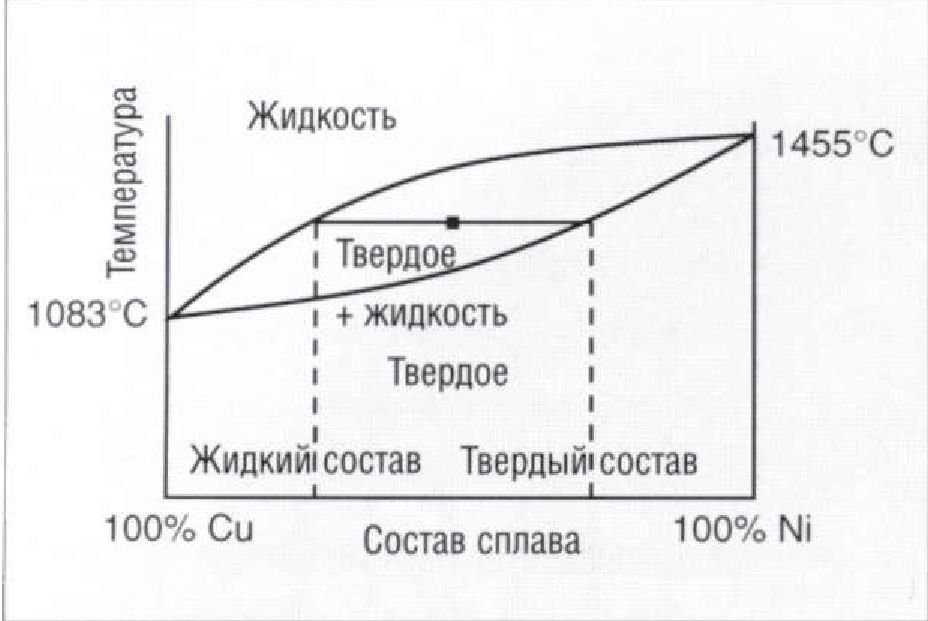
Рис. 1.5.8. Фазовая диаграмма равновесия для системы Cu-Ni, соотношение компонентов в которой 50 Си : 50 Ni при 1300°С дает составы, обогащенные медью в жидком расплаве и обогащенные никелем - в твердом состоянии
ратурами плавления чистои меди и чистого никеля, на самом деле это не так. Сразу сложно понять, почему на диаграмме появляется область, в которой присутствуют одновременно жидкий расплав и твердая фаза. Линия, которая отделяет область только жидкой фазы от области, состоящей из жидкости и твердой фазы, называется ликвидусом или линией ликвидуса, а линия, отделяющая смесь жидкости и твердого от области, в которой присутствует только твердая фаза, известна под названием солидуса или линией солидуса.
При твердении чистого металла, переход от жидкого в твердое состояние происходит при вполне определенной температуре; такой температурой является характеризующая физические свойства данного металла температура плавления. Если для чистого металла построить кривую в координатах температура — время, она будет иметь вид, представленный на Рис. 1.5.9.
Протяженность плато на кривой соответствует периоду, в течение которого происходит твердение металла, а линии ликвидус и солидус совместились в одной точке. Причиной образования плато является высвобождение энергии (в форме тепла) при твердении материала, которая поддерживает постоянную температуру металла при его твердении. Эта энергия называется скрытой теплотой плавления.
При смешивании двух металлов для получения сплава, кривая охлаждения выглядит иначе (Рис. 1.5.10), поскольку твердение сплава происходит не при одной температуре, а в определенном температурном интервале. Ликвидус и солидус становятся раздельными точками на кривой охлаждения (Рис. 1.5.10).
Причина расширения интервала температур, в котором происходит переход от твердого состояния к жидкому в сплаве меди и никеля, заключается в том, что атомы этих металлов не являются идентичными.
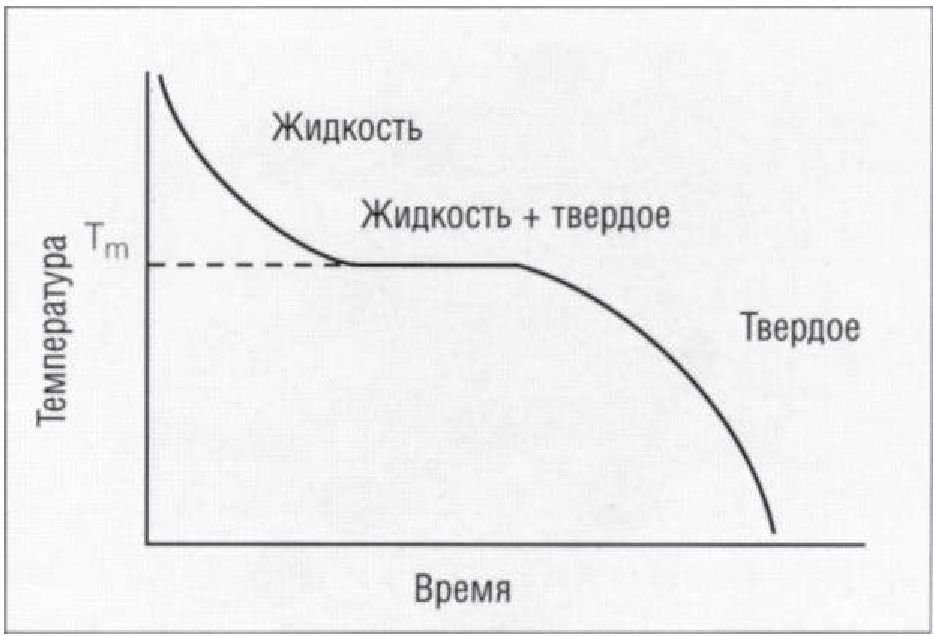
Рис. 1.5.9. Кривая охлаждения расплава чистого металла
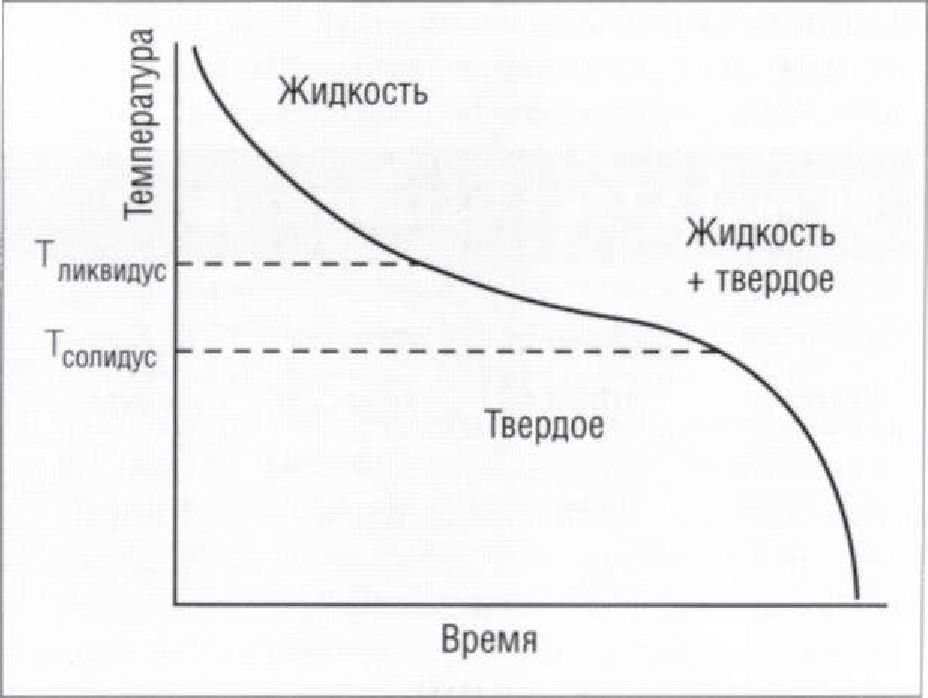
Рис. 1.5.10. Кривая охлаждения сплава
Следовательно, в области, находящейся между разными температурами плавления этих двух металлов, остается жидкий расплав, обогащенный медью, имеющий более низкую точку плавления, и появляется твердая фаза, обогащенная никелем с более высокой точкой плавления. В данной температурной области эти фазы представляют собой самые стабильные соединения.
Например, для состава, содержащего 50% меди и 50% никеля, при температуре 1300°С, в твердом никеле может содержаться не более 37 массовых процентов меди. Следовательно, любые лишние атомы меди, выходящие за пределы уровня 37%, переходят в жидкое состояние и смешиваются с оставшимся никелем. Такая смесь твердого и жидкости обладает более низкой свободной энергией, чем однофазное состояние.
Положение линий солидус и ликвидус связано с пределами растворимости, и на этом основано построение фазовых диаграмм. Вычерчивая для разных
композиций по эмпирическим данным серию кривых охлаждения, представленных на Рис. 1.5.11, можно построить фазовую диаграмму, схематически представленную на Рис. 1.5.8. По мере снижения температуры состава 50 : 50 (50% меди и 50% никеля), растворимость меди в никеле повышается, и это будет продолжаться до температуры ~1220°С. При этой температуре вся имеющаяся медь растворится в никеле с образованием однофазного твердого раствора, обладающего наиболее стабильной структурой.