При низких концентрациях меди в композиции серебро-медь, вся присутствующая медь растворится в серебре, при этом образуется только одна фаза. Максимальная растворимость меди в серебре составляет 8,8 массовых процентов при температуре 780°С.
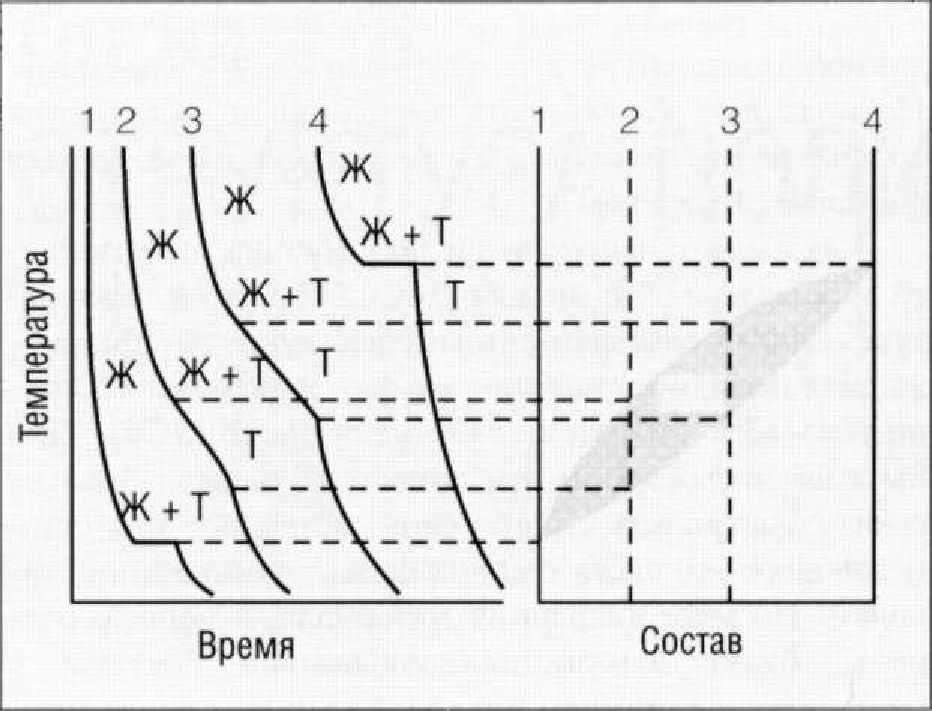
Рис. 1.5.11. Построение фазовой диаграммы
При понижении температуры растворимость меди в серебре также значительно понижается, и избыток меди как бы выпадает в осадок, образуя вторую, р-фазу.
Аналогично поведет себя серебро при его низкой концентрации в составе сплава серебро-медь. В этом случае ограниченная растворимость серебра в меди также приведет к образованию двухфазной структуры.
Интересной и важной частью фазовой диаграммы системы Ag — Си является снижение температуры ликвидуса при получении композиции, состоящей из 72 частей серебра и 28 частей меди (72Ag:28Cu). При температуре 780°С сплав будет состоять из трех фаз: жидкой фазы, ос-фазы и Р-фазы. Эта точка называется точкой эвтектики или эвтектической точкой, а температура, при которой существуют все три фазы — температурой эвтектики или эвтектической температурой. Подобные композиции называются эвтектическими составами, или сплавом эвтектического состава.
При охлаждении жидкости эвтектического состава, она сразу же превращается в две твердые фазы, без образования промежуточной смеси жидкости с твердым — того, что наблюдается у сплавов неэвтектического состава. Это свойство некоторых систем сплавов можно использовать для образования материалов с низкой температурой плавления, например, припоев.
Аналогично тому, как при эвтектической температуре из одной жидкой фазы образуются две твердые фазы, такие же превращения (образование двух фаз из одной) могут наблюдаться и в твердом состоянии.
Примером такого превращения служит система Fe - С, фазовая диаграмма которой представлена на Рис. 1.5.13. Для композиции 0,8С : 99,2Fe, при температуре 723°С твердый раствор, у-фаза, переходит в твердый раствор углерода в железе, ос-фазу, и карбид железа, Fe
C. Такой переход называется эвтектической реакцией, и отличается от эвтектики тем, что все три фазы существуют в твердом виде.
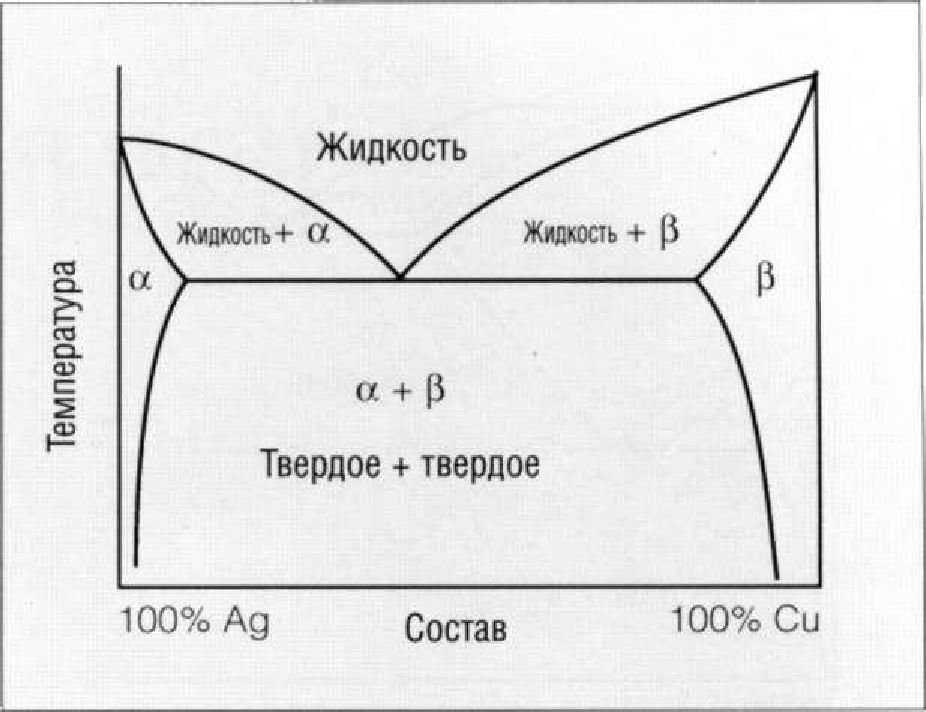
Рис. 1.5.12. Фазовая диаграмма равновесия для системы Ag-Cu